高二化学选修4检测题及答案
检测题是高二化学的主要考察方式,即便是选修内容,锻炼也不能少。下面是小编为您带来的高二化学选修4检测题及答案,试试看自己能记忆多少?
高二化学选修4检测题:
可能用到的部分原子量:H—1 C—12 O—16 S—32 Na—23
第I卷(共36分)
一、单选题(本题包括6小题,每小题4分,共24分。每小题只有一个选项符合题意)
1、未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是
①天然气 ②太阳能 ③风能 ④石油 ⑤煤 ⑥生物质能 ⑦核能 ⑧氢能
A.①②③④ B.②③⑥⑧
C.①②⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
2、氨水有下列平衡:NH3·H2O

NH4+ + OH– 当其它条件不变时,改变下列条件,平衡向左移动,且c(NH4+)增大的是
A.加NaOH B.加盐酸 C.加NH4Cl D.加热

3、铜锌原电池(如图)工作时,下列叙述错误的是
A.正极反应为:Cu2++2e–= Cu
B.电池反应为:Zn+Cu2+=Zn2+ +Cu
C.在外电路中,电子从负极流向正极
D.盐桥中的K+移向ZnSO4溶液
4、在由水电离产生的c(H+)=1×10–14mol/L的溶液中,一定可以大量共存的离子组是
A.K+、Ba2+、Cl–、NO3– B.Na+、Ca2+、I–、NO3–
C.NH4+、Al3+、Br–、SO42– D.K+、Na+、HCO3–、SO42–
5、已知:Ksp(AgCl)=1.8×10—10,Ksp(AgI)=1.5×10—16 ,Ksp(AgBr)=7.7×10—13,则下列难溶

盐的饱和溶液中,Ag+浓度大小顺序正确的是
A.AgCl>AgI> AgBr B.AgCl> AgBr>AgI
C.AgBr >AgCl>AgI D.AgBr >AgI>AgCl
6、已知:△G=△H-T△S,△H为焓变,T为热力学温度,△S熵变,当△G<0时反应能自发进行,△G>0时反应不能自发进行,据此,下列叙述中正确的是
A.熵变大于零的反应肯定能自发进行
B.焓变小于零的反应肯定能自发进行
C.焓变大于

零的反应肯定不能自发进行
D.焓变小于零且熵变大于零的反应一定能自发进行
二、双选题(本题包括2小题,每小题6分,共12分。每小题有两个选项符合题意。若只选一个且正确的给3分,选两个且都正确的给6分,但只要选错一个,该题为0分)
7、反应mA(固)+nB(气) eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是

A.到平衡后,加入催化剂C%不变
B.达到平衡后,若升温,平衡右移
C.化学方程式中n>e+f
D.达到平衡后,增加A的质量有利于平衡向右移动
8、草酸是二元弱酸,草酸氢钾溶液呈酸性。在0.1 mol · L-1 KHC2O4溶液中下列关系正确的是

第Ⅱ卷(非选择题共64分)

9、(1)(8分)2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ/mol。
请回答下列问题:
①图中A点表示:
C点表示:
E的大小对该反应的反应热 (填“有”或“无”)
影响。
②图中△H= kJ/mol。
(2)(6分)由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量(25℃、101 kPa下测得)
①写出该反应的热化学方程式:
②若1 mol水蒸气转化为液态水放热45kJ,则反应H2(g) +1/2
O2(g) = H2O( l )的
ΔH = kJ/mol。氢气的燃烧热为ΔH = kJ/mol。
10、(16分)有可逆反应Fe(s)+CO2(g)=FeO(s) + CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2 。
(1)能判断该反应达到平衡状态的依据是 (双选,填序号)。
A.容器内压强不变了 B.c(CO)不变了
C.v正(CO2)=v逆(C
O) D.c(CO2)=c(CO)
(2)该反应的正反应是_________(选填“吸热”、“放热”)反应。
(3)写出该反应的平衡常数表达式__________。若起始时把Fe和CO2放入体积固定的密闭容器中,CO2的起始浓度为2.0mol/L,某温度时达到平衡,此时容器中CO的浓度为1.0 mol/L,则该温度下上述反应的平衡常数K=__________(保留二位有效数字)。
(4)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,如果改变下列条件,反应混合气体中CO2的物质的量分数如何变化(选填“增大”、“减小”、“不变”)。
①升高温度__________;②再通入CO___________。
(5)该反应的逆反应速率随时间变化的关系如下图:
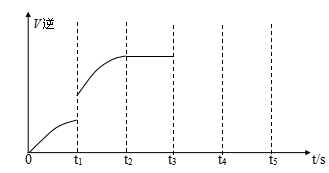
①从图中看到,反应在t2时达平衡, 在t1时改变了某种条件,改变的条件可能是(填序号)__ ___。(单选)
A.升温
B.增大CO2浓度
②如果在t3时从混合物中分离出部分CO,t4~ t5时间段反应处于新平衡状态,请在图上画出t3~ t5的V(逆)变化曲线
11、(16分)海水中蕴藏着丰富的资源,海水综合利用的流程图如下:

(一)某化学研究小组用右图装置模拟步骤I电解食盐水
(用铁和石墨做电极)。
(1)a电极材料是 (填铁、石墨),
其电极反应式为 。
(2)当阴极产生11.2mL气体时(标准状况),该溶液的
pH为 (忽略反应前后溶液体积的变化)。
(二)卤水中蕴含着丰富的镁资源,就MgCl2粗产品的提纯、镁的冶炼过程回答下列问题:
已知MgCl2粗产品的溶液中含有Fe2+、Fe3+和Al3+。
下表是生成氢氧化物沉淀的pH:
物质
Fe###(OH)###3
Fe###(OH)###2
Al(OH)###3
Mg###(OH)###2
开始沉淀pH
2.7
8.1
3.8
9.5
完全沉淀pH
3.7
9.6
4.8
11.0
(3)把MgCl2粗产品的溶液中的Fe2+转化为Fe3+,可选用的物质是________(填序号,下同),加入 调节溶液的pH,充分反应后过滤,可得MgCl2溶液。
a.KMnO4 b.H2O2 c.MgO d.NaOH
(4)步骤Ⅲ由MgCl2·H2O获得MgCl2的操作是: 。
(三)制取工业溴:
(5)步骤Ⅳ中已获得Br2,步骤Ⅴ中又将Br2还原为Br-,其目的是 。
(6)写出步骤Ⅴ用SO2水溶液吸收Br2的离子方程式: 。
12、(18分)甲乙两同学对保存已久的Na2SO3试剂进行试验探究。
取适量Na2SO3样品于洁净烧杯中,加入适量蒸馏水,充分搅拌全部溶解。
(1)测上述溶液的PH值,其PH值>7,原因是(用离子方程式表示)
(2)取少量上述溶液于试管中,加入硝酸钡溶液生成白色沉淀,再加入盐酸,白色沉淀不溶解,甲认为已变质,乙认为他的结论不科学,理由是
(3)假设试剂由Na2SO3和Na2SO4组成,设计试验方案,进行成分检验,他们决定继续探究,请在答题卡上写出实验步骤、预期现象和结论。
限选试剂及仪器:稀盐酸、稀硝酸、氯化钡溶液,品红溶液,酸性高锰酸溶液,NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
实验步骤
预期现象和结论
步骤###1###:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置。
步骤###2###:取适量步骤###1###所得溶液于试管中,加入少量的###溶液。
若溶液褪色,说明其有
若溶液不褪色,说明其中没有
步骤###3###:###再取适量步骤###1###所得溶液于另一试管中,先加入足量的稀盐酸,再滴
加###溶液。
如果有白色沉淀生成,则说明其中有###,已经变质。
如果没有白色沉淀生成,则说明其中
没有
(4)经实验检验后,确实已变质,现准确测定其中Na2SO3的含量。实验如下:
①配制250ml 约0.2mol•L-1 Na2SO3溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水溶解,将溶液转入 ,洗涤,定容,摇匀。
②滴定:准确量取25.00ml Na2SO3所配制溶液于锥形瓶中,将 0.05mol•L-1酸性高锰酸钾装入50ml (填酸式或碱式)滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗KMnO4VmL。
③计算Na2SO3的质量分数= (只列出计算式,不要求算出结果)
高二化学选修4检测题答案:
题号
1
2
3
4
5
6
7
8
答案
B
C
D
A
B
D
AC
AD
9、(1)(8分)①

反应物的总能量; 生成物的总能量; 无; -198 。(每空2分) (2)(6分)H2 ( g ) +1/2
O2 ( g )=H2O ( g ) ΔH =―241.8 kJ/mol (2分)。
( 或2H2 (g) +O2(g)=2H2O(g) ΔH =―483.6kJ/mol )。

―286.8 (2分); ―286.8 (2分)
10、(1)B、C(2分)
(2)吸热(2分)
(3)k=c(CO)/c(CO2)), 1.0(各2分)
(4)减小(2分) 不变(2分)
(5)①A(2分) ②如图(2分)
11、(1)石墨(2分) 2Cl--2e-==Cl2↑ (2分)
(2)12(2分) (3)b ;c(4分)
(4)将MgCl2·6H2O在干燥的HCl气流中加热 (2分)
(5)富集溴元素(2分)
(6)Br2+SO2+2H2O=4H++SO42-+2Br-(2分)
12、(1)SO32-+H2O=HSO3-+OH-(2分)
(2)溶液中的NO3-和H+在一起有强氧化性,会把亚硫酸钡氧化成硫酸钡(2分)
(3)(8分)
实验步骤
预期现象和结论
步骤###2###:取适量步骤###1###所得溶液于试管中,加入少量的###酸性高锰酸溶液###(2分)
若酸性高锰酸溶液褪色,说明中有###Na###2###S###O###3###(1分)
若酸性高锰酸溶液不褪色,说明中没有###Na###2###S###O###3###(1分)
步骤###3###:###再取适量步骤###1###所得溶液于另一试管中,先加入足量的稀盐酸,再滴加###氯化钡###溶液(2分)
如果有白色沉淀生成,则说明其中有###Na###2###S###O###4###,已经变质(1分)
如果没有白色沉淀生成,则说明没有###Na###2###S###O###4###(1分)
(3)(6分)
①250mL容量瓶
②酸式
③计算Na2SO3的质量分数=5×0.05×10×126V/2000W×100%
以上就是小编带来的高二化学选修4检测题及答案全部内容,希望你能喜欢。
高二化学选修4检测题相关文章推荐:
1.高二化学选修4期末试卷及答案
2.高二化学选修4期末测试及答案
3.高二新课标人教版化学选修4章节练习题及答案
4.高二化学选修4第一章测试题及答案
5.高中化学选修4练习题及答案
6.高中化学选修4经典例题及答案
7.高二化学选修4第四章练习题及答案
8.高二化学选修4第一章测试及答案
9.高中化学选修4第三章测试及答案
10.高中化学选修四练习题及答案