2016高中会考化学测试卷
相关话题
高中会考是为高考做的准备。小编给同学们整理了2016高中会考化学测试卷,祝大家考试顺利!
2016高中会考化学测试卷
一、选择题(每题有1-2个正确答案)(5×10分)
[ ]1.查阅资料发现,金属钠不仅能跟氧气和水反应,还能跟多种其它物质发生反应,其中包括与酒精在常温下反应。要研究金属钠跟酒精反应的性质以及它与水反应的异同点,下列的研究方法中没有用到的是
A.实验法 B.观察法 C.分类法 D.比较法
[ ]2.下列关于胶体的叙述不正确的是 A.布朗运动是胶体微粒特有的运动方式,可以据此把胶体和溶液、悬浊液区别开来
B.光线透过胶体时,胶体发生丁达尔现象
C.用渗析的方法净化胶体时,使用的半透膜只能让较小的分子、离子通过
D.胶体微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象
[ ]3.金属材料在日常生活以及生产中有着广泛的运用。下列关于金属的一些说法不正确的是
A.合金的性质与其成分金属的性质不完全相同
B.工业上金属Mg、Al都是用电解熔融的氯化物制得的
C.金属冶炼的本质是金属阳离子得到电子变成金属原子
D.越活泼的金属越难冶炼
[ ]4.某同学进行实验,出现小气球鼓起来的现象,则使用的固体和液体试剂可能是( )
A、铜与浓硫酸 B、铁与浓硫酸 C、铝和氢氧化钠溶液 D、二氧化锰和浓盐酸
[ ]5.下列各组的两种溶液中,分别加入足量氨水,观察到的现象相同的是( )
A.FeCl3 AlCl3 B.NaCl BaCl2 C.MgCl2 CuCl2 D.FeCl2 FeCl3
[ ]6.已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是
A.Z元素的原子半径可能比Y元素的小
B.Z元素的最高化合价可能比Y元素的高
C.W的气态氢化物的稳定性一定比Y的强
D.Z的最高价氧化物的水化物的酸性一定比W的强
[ ]7.NA代表阿伏加德罗常数,下列说法正确的是
A.9gD2O中含有的电子数为5NA B.1molMgCl2中含有的离子数为2NA
C.1molCH4分子中共价键总数为4NA
D.7.1g C12与足量NaOH溶液反应转移的电子数为0.2NA
[ ]8.下列各组离子一定能大量共存的是
A、含有大量Fe3+的溶液中:NH4+、Na+、Clˉ、SCNˉ
B、在强碱溶液中:Na+、K+、AlO2ˉ、CO32-
C、在c(OH—)=10-13mol·L-1的溶液中:NH4+、Al3+、SO42-、NO3ˉ
D 无色溶液中: K+ Cl— MnO4— SO42—
[ ]9.下列离子方程式中,正确的是
A.向Mg(HCO3)2溶液中加入过量的NaOH溶液
B.向Fe(NO3)2溶液中加入稀的氢碘酸:
C.足量的CO2通入稀的碳酸钠溶液中:CO2+CO
D.向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO反应完全 2Ba2++4OH—+Al3++2SO
[ ]10.等物质的量的主族金属元素的单质A、B、C,分别与足量的稀盐酸反应,同条件下得氢气的体积依次为VA、VB、VC,已知VB=2VC,VA=VB+VC,则在C的生成物中该金属元素的化合价为
A.+1 B.+2 C.+3 D.+4
二、非选择题 (70分)
11.(12分)工业上制取CuCl2的生产流程如下:
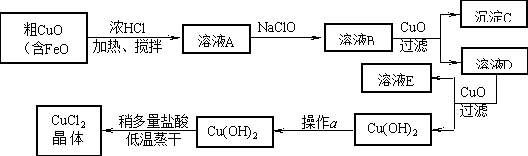
请结合下表数据,回答下列问题:
物 质Fe(OH)2Cu(OH)2Fe(OH)3
溶度积/25℃8.0×10-162.2×10-204.0×10-38
完全沉淀时的pH范围≥9.6≥6.43~4
⑴ 溶液A中加入NaClO的目的是 ;
⑵ 在溶液B中加入CuO的作用是 ;
⑶ 操作a的目的是 ;
⑷ 在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是 。
12.(15分)某待测溶液中可能含有Fe2+、Fe3+、Ag+、Al3+、Ba2+、Ca2+、NH4+等离子,进行如下实验(所加酸、碱、氨水、溴水CO2都是过量的)。
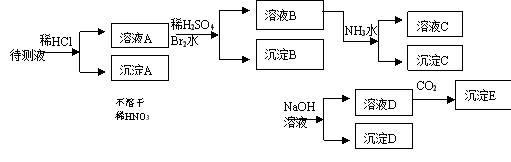
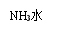
根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子: 。
理由是: 。
(2)写出沉淀D的分子式: 。
(3)写出从溶液D生成沉淀E的反应的离子方程式: 。
(4)写出从溶液B生成沉淀C的反应的离子方程式:
___________________ 。
13.(20分)下表为元素周期表的一部分,请回答有关问题:
IAIIAIIIAIVAVAVIAVIIA0
2①②
3③④⑤⑥⑦⑧
4⑨⑩
(1)⑤和⑧的元素符号是 和 ;
(2)表中最活泼的金属是 ,非金属最强的元素是 ;(填写元素符号)
(3)表中能形成两性氢氧化物的元素是 ,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的离子方程式:
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:
14.(11分)A~J是中学化学中常见的几种物质,它们之间的转化关系如下图所示。已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F化合生成,J可作禽流感、SARS等病毒的杀菌消毒剂。

(1)分别写出B、D的电子式:______________ _____、______________________。
(2)写出反应⑦的离子方程式:__________。
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式: 。
15.(12分)将32.64g铜与140ml一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为 L,NO2的体积为 L。
(2)待产生的气体全部释放后,向溶液加入a mol·L-1的NaOH溶液,恰好使溶液全部转化成沉淀,则原硝酸溶液的浓度为 mol/L。