高一化学必修1《氮的氧化物》期末练习试题
对于化学的学习,在小编看来,想要提升自己的化学学习成绩的一种重要方法就是多做试题!下面是小编整理的人教版高一化学必修1《氮的氧化物》期末练习试题以供大家学习参考。
人教版高一化学必修1《氮的氧化物》期末练习试题
选择题
如图,将A、B两瓶中的无色气体混合后,集气瓶中充满红棕色的气体,则对A、B瓶中气体成分判断正确的是 ( )
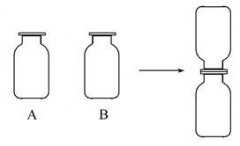
A.A是NO,B是空气 B.A是NO2,B是水蒸气
C.A是NH3,B是HCl D.A是NO,B是水蒸气
工业废气中氮氧化物是主要的大气污染源之一,已知:
2NO2+2NaOH====NaNO3+NaNO2+H2O
NO2+NO+2NaOH====2NaNO2+H2O
现有amol NO2和bmol NO的混合气体,若用足量的NaOH溶液将其完全吸收,则a和b必须满足的关系是
A.a=3bB.a=b
C.a≥bD.任意比例
已知HNO3具有强氧化性,鉴别二氧化氮与溴蒸气,下列可选用的试剂是 ( )
A.淀粉碘化钾B.蒸馏水
C.氢氧化钠D.硝酸银
下列有关氮气的叙述中,错误的是 ( )
A.镁在空气中燃烧除生成氧化镁外还生成氮化镁
B.在雷雨天,空气中的N2和O2可反应生成NO
C.氮气既可作氧化剂又可作还原剂
D.1 mol N2可与3 mol H2完全反应生成2 mol NH3
对汽车尾气的处理有人提出下列做法:在马路上铺设“光触媒”(如二氧化钛)物质,将空气中的氮氧化物、一氧化碳、二氧化硫等污染物在催化剂表面转化、分解成对人体、环境基本无害的物质。下列有关说法正确的是 ( )
A.此法可将汽车尾气中的CO在催化剂表面氧化生成CO2
B.此法可将汽车尾气中的NOx在催化剂表面氧化生成N2
C.此法可将汽车尾气中的二氧化硫还原成三氧化硫
D.此法是解决城市空气污染的唯一途径
反应NO+O2+NO2+H2O HNO3(未配平)是一个有多组化学计量数(即系数)的化学方程式,当O2有
HNO3(未配平)是一个有多组化学计量数(即系数)的化学方程式,当O2有
被NO还原时,此反应各物质的化学计量数为
A.4,9,24,14,28B.1,1,1,1,2
C.8,9,12,10,20D.任意数均可
已知某氮的氧化物中氧元素的质量分数为0.696,则其化学式是( )
A.NOB.NO2C.N2O4D.N2O3
在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法错误的是 ( )
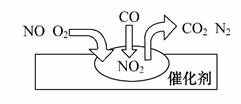
A.NO2是该过程的中间产物
B.汽车尾气的主要污染成分包括CO和NO
C.NO和O2必须在催化剂表面才能反应
D.催化转化总反应式为2NO+O2+4CO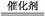 4CO2+N2
4CO2+N2
某集气瓶内装的混合气体呈红棕色,加入足量蒸馏水,盖上玻璃片振荡得橙黄色溶液,气体颜色消失,再打开玻璃片后,瓶中气体又变为红棕色,该混合气体可能是 ( )
A.N2、NO2、Br2B.NO2、NO、N2
C.NO2、NO、O2D.N2、O2、Br2
下列关于NO2和SO2的说法错误的是 ( )
A.NO2是一种红棕色、有毒、有刺激性气味的气体
B.NO2和SO2溶于水后所得的溶液都呈酸性
C.空气中的N2在闪电时,直接生成NO2
D.SO2是一种无色、有刺激性气味的气体,能够漂白草帽等物质
某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是 ( )
A.肯定有SO2和NO
B.肯定没有O2和NO2,可能有Cl2
C.可能有Cl2和O2
D.肯定只有NO
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。已知N5是可用作烈性炸药的一种分子,下列关于N4、N5的说法正确的是 ( )
A.相同质量的N4、N5分子其原子数之比为5∶4
B.N5、N4与N2互为同素异形体
C.N4、N5均属于新型的化合物
D.N5的摩尔质量为70
事实上,很多非金属氧化物在一定条件下都能与Na2O2反应,且反应极有规律。如Na2O2+SO2====Na2SO4,2Na2O2+2SO3====2Na2SO4+O2。据此,你认为下列反应方程式中正确的是 ( )
①2Na2O2+2N2O5====4NaNO3+O2↑
②Na2O2+2NO2====2NaNO2+O2
③2Na2O2+2N2O3====4NaNO2+O2
④Na2O2+N2O4====2NaNO3
A.①②B.②③C.③④D.①④
实验题
某课外活动小组探究镁与CO2、NO2的反应。
(1)实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应解释该现象 。
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测:写出Mg与NO2反应的化学方程式 。
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)
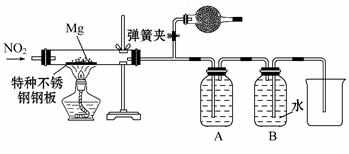
资料信息:2NO2+2NaOH====NaNO3+NaNO2+H2O。
①装置A中的试剂是 。
②干燥管和装置B的作用分别是 。
③实验开始时正确的操作步骤是 。
a.通入NO2
b.打开弹簧夹
c.点燃酒精灯
d.当硬质玻璃管充满红综色气体后,关闭弹簧夹
已知:Cu+4HNO3(浓)====Cu(NO3)2+2NO2↑+2H2O。为探究如何尽可能多地使NO2被水吸收,某活动小组设计并完成了以下实验。
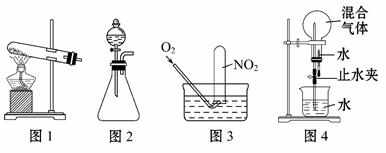
(1)活动小组同学利用铜与浓硝酸反应制取NO2、过氧化氢溶液与MnO2制取O2。
①根据反应原理他们选用了相同的装置 (填“图1”或“图2”)分别制取NO2和O2。
②写出铜与浓硝酸反应的离子方程式 。
③过氧化氢溶液与MnO2制取O2时,MnO2的作用是
_________________________________________________________________。
④收集NO2可采用的方法是 。
(2)活动小组的同学做了如下准备:用气囊收集好纯净的O2;收集了一试管NO2;用干燥的烧瓶收集了一定比例的NO2和O2混合气体。
①为了尽可能多地使NO2被水吸收,并达到较好的实验效果,利用图3吸收气体时,用气囊通入O2与直接利用制气装置制取并通入O2相比,其优点是
②利用图4吸收气体时,其操作和现象为
③NO2、O2、H2O反应的产物为硝酸,反应中NO2和O2物质的量之比a∶b= ;标准状况下,若图4中混合气体NO2和O2比例为a∶b,当混合气体全部被吸收时所得溶液物质的量浓度为 mol·L-1(保留两位有效数字)。
填空题
今年我国多个城市遭雾霾天气,这表明污染严重,空气质量下降。因此研究NO2、SO2、CO等大气污染气体的处理具有重要现实意义。
(1)NO2可用水吸收,相应的化学反应方程式为 。
(2)利用反应6NO2+8NH3 7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是 L。
7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是 L。
(3)硝酸工业尾气中含NO和NO2气体,常用NaOH溶液来吸收,反应方程式为NO+NO2+2NaOH====2NaNO2+H2O,该反应中氧化剂和还原剂的物质的量之比是 。
(4)SO2是形成酸雨的主要物质,可以用氨水吸收消除污染,写出过量氨水与SO2反应的离子方程式 。
氮元素的化合价较多,负价态氮与正价态氮之间发生氧化还原反应时会有氮气产生。下面是甲、乙两位学生提出的两种制备少量氮气的实验方案(箭头表示气体的流向)。
甲:空气→碱石灰→红磷(点燃)→水→铜粉(灼热)→集气瓶
乙:NH4NO2(加热)→浓硫酸→镁粉(灼热)→集气瓶(提示:NH4NO2 N2↑+2H2O)
N2↑+2H2O)
回答下列问题:
(1)甲、乙两位学生的实验方案是否能制氮气?
甲 、乙 (填“能”或“不能”)。
(2)具体说明不能制取氮气的原因并纠正(若两种方案都能制氮气,此小题不用回答) 。
(3)甲方案中碱石灰和乙方案中浓硫酸可否交换位置?说明理由: